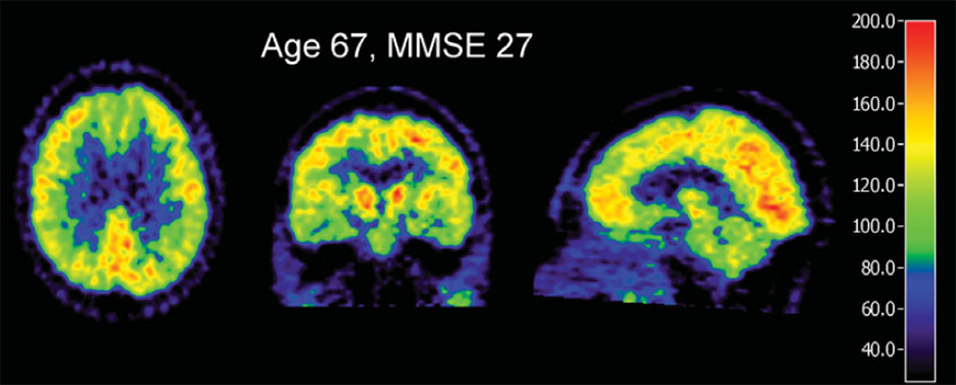
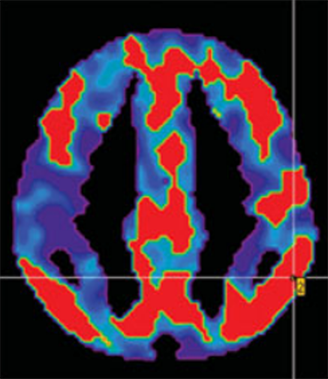
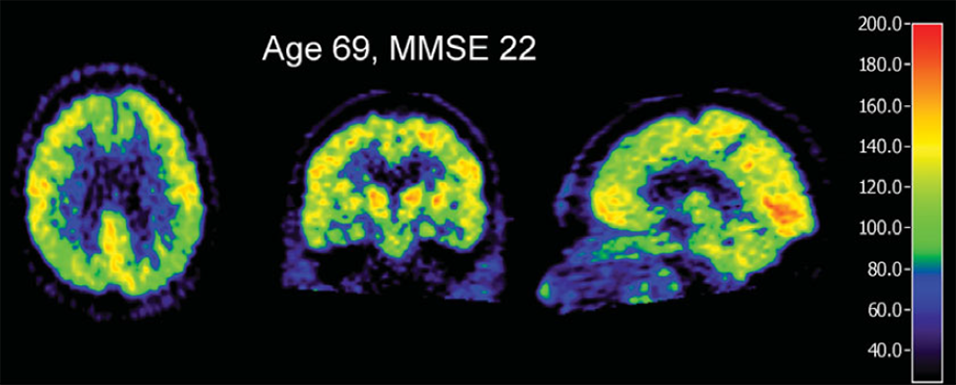
Doença de Alzheimer
Explorando o futuro da pesquisa,
diagnóstico e cuidados da Doença de Alzheimer

Doença de Alzheimer
Passado, presente e futuro da Doença de Alzheimer
A Doença de Alzheimer (DA) é uma entidade biológica definida pela presença de placas amiloides e emaranhados neurofibrilares da tau (NFT).1
- É uma doença contínua que começa com a aparição de patologia cerebral em indivíduos assintomáticos e progride por meio de estágios crescentes de fardo patológico, levando, por fim, a aparição e progressão de sintomas clínicos.2,3
- A doença é diagnosticada in vivo por anormalidades em biomarcadores principais relacionados à patologia amiloide na presença de comprometimento cognitivo.1,3
Principais sinais característicos da Doença de Alzheimer2,4,5
Clique nos componentes celulares para saber mais
Responda à seguinte pergunta para continuar
Que porcentagem de pacientes você diagnostica normalmente para DA nos seguintes grupos etários?
O modelo de degeneração amiloide-tau (AT(N))
- O modelo AT(N) define a Doença de Alzheimer de acordo com a positividade de biomarcadores para amiloide (A), tau (T) e neurodegeneração (N)1,14
- O modelo é flexível para acomodar a complexidade da Doença de Alzheimer a medida que novos biomarcadores fiquem disponíveis, como os para lesões vasculares, neuroinflamação, oxidação e dano mitocondrial1,14
- O sistema AT(N) possui tanto marcadores LCR quanto de imagens em cada um dos três grupos, de modo que diferentes biomarcadores possam ser usados dependendo do teste disponível1
- Critérios revisados (atualização NIA-AA 2023), discutem os biomarcadores principais 1 e 2 (para amiloide e tau) e incluem um modelo expandido do AT(N) denominada AT(NIVS), para incluir três novas categorias de biomarcadores: mecanismos inflamatórios/imunes (I), lesão vascular cerebral (V) e sinucleinopatia (S)3
- Os testes de biomarcadores devem sempre ser solicitados ou interpretados considerando o contexto clínico. O julgamento clínico é necessário para avaliar se a Doença de Alzheimer é a causa (ou um componente dominante) da apresentação sintomática do paciente
Modelo AT(NIVS) para biomarcadores na doença de Alzheimer (para diagnóstico, estadiamento, prognóstico ou indicador de efeito do tratamento)3
- Os biomarcadores principais 1 incluem PET amiloide e aqueles que se tornam anormais ao mesmo tempo (A, T1 ou categorias de taxa híbrida); para diagnóstico de DA em pessoas assintomáticas e sintomáticas3
- Os biomarcadores principais 2 incluem PET tau, 149 pT205, MTBR-tau243 e tau não fosforilado que se tornam anormais em um estágio mais avançado da DA e que estão intimamente ligados ao início dos sintomas3

A
Placas amiloides
(amiloide agregado)
Biomarcador principal
Proteinopatia Amiloide-beta
Principal 1
- LCR Aβ42
- Taxa de Aβ42/Aβ40
- PET amiloide

T
Emaranhados neurofibrilares
(tau agregada)
Biomarcador principal
T1: Analitos de
fragmentos solúveis da tau refletindo a
reação ao amiloide solúvel ou placas
de amiloide.
T2: imagem PET tau ou analitos fluidos indicando proteinopatia da tau
Principal 1 (T1)
- LCR ou plasma p‑tau217, p‑tau181, p‑tau231
Principal 2 (T2)
- LCR ou plasma pT205, CSF MTBR‑tau243, fragmentos de tau não fosforilados
- PET Tau
Taxas de A e T:
- LCR p-tau181/Aβ42, t-tau/Aβ42
- Sangue p‑tau217/np‑tau217
N
Neurodegeneração
- RM ou TC
- PET FDG
- LCR tau total
- LCR NfL
- NfL sanguíneo
I
Inflamação
(ativação do astrócito)
- LCR GFAP
- Plasma GFAP
V
Lesão vascular cerebral
- Imagens de infarto anatômico,alteração de substância branca (microangiopatia), abundância de espaços perivasculares dilatados
S
Sinucleinopatia
(alfa-sinucleína)
- LCR alfa‑Syn‑SAA†
Adaptado de Jack C R et al, 20181
and Alzheimer’s Association, 20233
†Analito fluido é somente informativo atualmente.
Desenvolvimento e interpretação do biomarcador amiloide e tau
- Vários biomarcadores sanguíneos (BMSs) estão em desenvolvimento, mas ainda não são amplamente utilizados na prática clínica.15
- PET amiloide e PET tau são atualmente usados principalmente para fins de pesquisa, embora estejam incluídos no processo diagnóstico em algumas clínicas15

Adaptado de Iaccarino L et al, 202315
Fatores de risco modificáveis relacionados ao estilo de vida
- Aproximadamente 40% de todas as demências estão ligadas a fatores de risco modificáveis relacionados ao estilo de vida.16
- Intervenções multidimensionais podem ajudar a prevenir o declínio cognitivo.16
O estudo FINGER identificou cinco domínios principais onde a intervenção poderia prevenir o declínio cognitivo em idosos sob risco.17
Estudo Finlandês de Intervenção Geriátrica para Prevenir o Comprometimento Cognitivo e a Deficiência (FINGER)17
Um ensaio clínico randomizado de 2 anos para avaliar uma abordagem multidimensional a fim de prevenir o declínio cognitivo em idosos sob risco da população geral (N = 1.260)
Guia nutricional
Exercício físico
Treinamento cognitivo
Atividades sociais
Gerenciamento de fatores de risco vasculares e metabólicos
DA: Doença de Alzheimer; AVD: atividades da vida diária; Alfa-Syn-SAA: Ensaios de amplificação de sementes de alfa-sinucleína; LCR: líquido cefalorraquidiano; TC: tomografia computadorizada; FDG: fluordeoxiglicose; GFAP: proteína glial fibrilar ácida; IWG: International Working Group; CCL: comprometimento cognitivo leve; RM: ressonância magnética; NFT: emaranhado neurofibrilar; NIA‑AA: National Institute on Aging and Alzheimer's Association; np‑tau: tau não fosforilada; PET: tomografia por emissão de pósitrons; p-tau: tau fosforilada; WMH: hiperintesidades da matéria branca
Referências
- Jack C R, Jr., Bennett D A et al. NIA-AA research framework: em direção a uma definição biológica da Doença de Alzheimer. Alzheimers Dement 2018;14(4):535-562
- Aisen P S, Cummings J et al. No caminho para 2025: entendendo o processo contínuo da Doença de Alzheimer. Alzheimers Res Ther 2017;9(1):60
- Jack C R Jr, Andrews J S et al. Critérios revisados para o diagnóstico e estadiamento da Doença de Alzheimer: Alzheimer's Association Workgroup. Alzheimers Dement 2024; doi:10.1002/alz.13859
- Alzheimer's Association. Fatos e números da Doença de Alzheimer 2023. Alzheimers Dement 2023;19(4):1598-1695
- Kinney J W, Bemiller S M et al. Inflamação como um mecanismo central na Doença de Alzheimer. Alzheimers Dement (N Y) 2018;4(1):575-590
- US Food and Drug Administration. Doença de Alzheimer precoce: desenvolvendo remédios para o tratamento. Guia para a indústria. Disponível em: fda.gov. Acessado em julho de 2024
- El-Hayek Y H, Wiley R E et al. A ponta do iceberg: avaliando os custos socioeconômicos globais da Doença de Alzheimer e demências relacionadas, bem como as implicações estratégicas para stakeholders. J Alzheimers Dis 2019;70(2):323-341
- Dubois B, von Arnim C A F et al. Biomarcadores da Doença de Alzheimer: papel no diagnóstico precoce e diferenciado e reconhecimento de variantes atípicas. Alzheimers Res Ther 2023;15(1):175
- Organização Mundial da Saúde. Demência. Disponível em: who.int. Acessado em julho de 2024
- Cummings J, Zhou Y et al. O funil do desenvolvimento de remédios para a Doença de Alzheimer, 2023. Alzheimers Dement (N Y) 2023;9(2):e12385
- Kate M T, Ingala S et al. Prevenção secundária da demência por Alzheimer: contribuições da neuroimagem. Alzheimers Res Ther 2018;10(1):112
- Kim K T. Punção lombar: considerações, procedimento e complicações. Encephalitis 2022;2(4):93-97
- Herholz K. Perfusão SPECT e PET FDG. Int Psychogeriatr 2011;23 Suppl 2:S25-31
- Bieger A, Rocha A et al. Biomarcadores de neuroinflamação no modelo AT(N) no contínuo da Doença de Alzheimer. J Alzheimers Dis 2023;10(3):401-417
- Iaccarino L, Burnham S C et al. Biomarcadores diagnósticos da patologia amiloide e tau na Doença de Alzheimer: uma visão geral dos testes para a prática clínica nos Estados Unidos e na Europa. J Prev Alzheimers Dis 2023;10(3):426-442
- Livingston G, Huntley J et al. Prevenção da demência, intervenção e cuidados: relatório 2020 da Comissão Lancet. Lancet 2020;396(10248):413-446
- Ngandu T, Lehtisalo J et al. O efeito da adesão à cognição em uma intervenção no estilo de vida multidimensional (FINGER). Alzheimers Dement 2022;18(7):1325-1334
HQ24SA00002 julho de 2024