La Comisión Europea aprueba BALVERSA®▼ (erdafitinib) para pacientes adultos con carcinoma urotelial no resecable o metastásico
- ComiteNetMD
- 13 de septiembre de 2024
- Oncología Médica
- 0 Comments
27/08/2024
Se trata del primer inhibidor de quinasa pan FGFR aprobado en el Espacio Económico Europeo, para adultos con carcinoma urotelial no resecable o metastásico y alteraciones susceptibles del FGFR3. La aprobación se basa en los resultados de THOR, que muestran una reducción del 36% en el riesgo de muerte con erdafitinib frente a quimioterapia1.
Johnson & Johnson ha anunciado que la Comisión Europea (CE) ha aprobado BALVERSA® ▼(erdafitinib) como monoterapia oral una vez al día para el tratamiento de pacientes adultos con carcinoma urotelial (CU) no resecable o metastásico (Cm), con alteraciones genéticas susceptibles en FGFR3 que han recibido previamente al menos una línea de tratamiento con un inhibidor de PD-1 o PD-L1 en el contexto no resecable o metastásico.
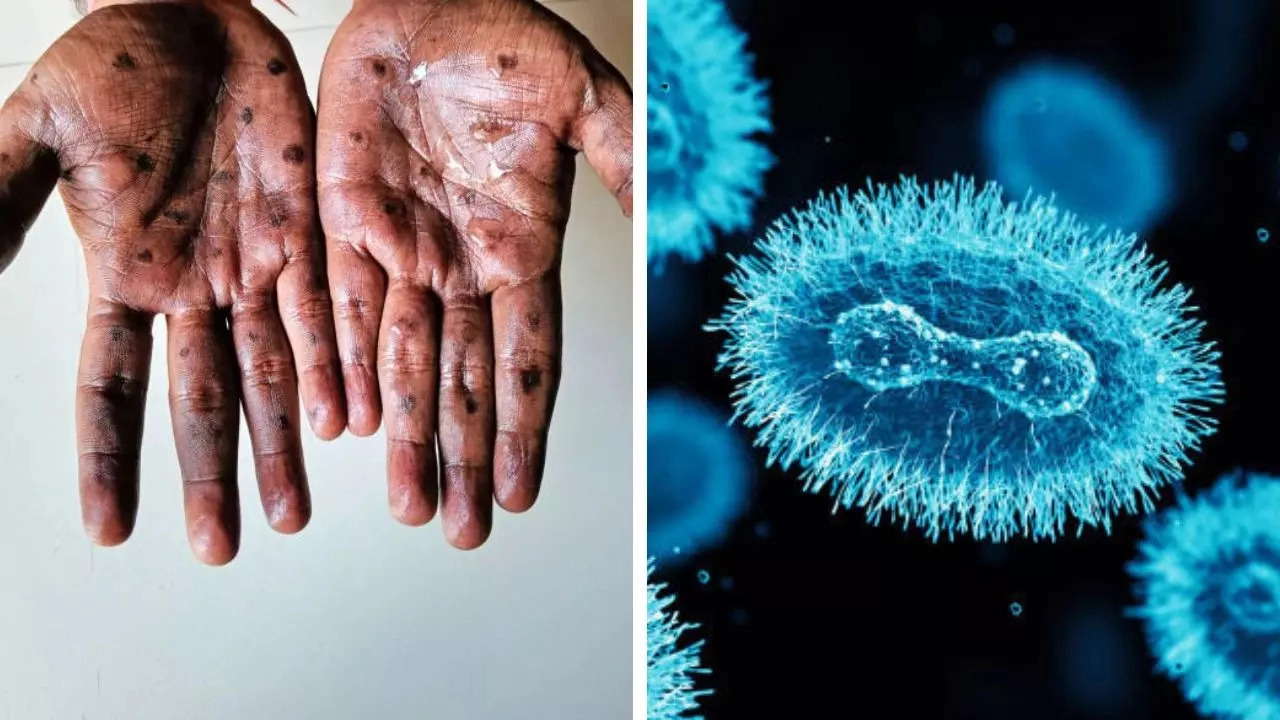
“El cáncer de vejiga es uno de los cánceres más comunes en Europa y la necesidad de nuevas opciones terapéuticas sigue siendo alta para las personas con carcinoma urotelial no resecable o metastásico”, ha señalado el Dr. Yohann Loriot, especialista del Instituto Gustave Roussy y la Universidad de Paris-Saclay (Francia*). “Erdafitinib es una nueva terapia dirigida, que ha demostrado una mejora significativa de la supervivencia global y de la supervivencia libre de progresión en los pacientes con alteraciones en FGFR3 que, hasta ahora, disponían de escasas opciones terapéuticas”.
Europa tiene la tasa más altas de cáncer de vejiga en comparación con el resto de continentes, con casi 250.000 pacientes diagnosticados en 2022, [i] lo que supone un aumento del 10% respecto a 2020. [ii] La forma más frecuente de cáncer de vejiga es el carcinoma urotelial (CU), [iii] y hasta un 20% de los pacientes con CU metastásico (CUm) presenta alteraciones en FGFR. [iv] El pronóstico de los pacientes con CUm sigue siendo pobre, con solo un 8% de las personas diagnosticadas en fase metastásica avanzada que sobrevive cinco años o más.2, 3
“Este importante hito pone de relieve el papel esencial de las terapias dirigidas en abordar la especificidad genética y als características patológicas de los pacientes con cáncer urotelial, y refuerza nuestra dedicación al avance e innovación de los tratamientos oncológicos dirigidos”, ha señalado la Dra. Henar Hevia, directora del Área de Oncología para Europa, África y Oriente Medio de Johnson & Johnson Innovative Medicine. “La aprobación de erdafitinib como tratamiento de precisión subraya la importancia de analizar FGFR en todos los pacientes con cáncer urotelial metastásico, así como la necesidad de un abordaje multidisciplinar para optimizar los resultados de cada paciente”.
Erdafitinib recibió la aprobación de la CE basada en los resultados de la cohorte 1 del estudio Fase 3 THOR (NCT03390504), que evalúa la eficacia y seguridad de erdafitinib (n=136) frente a quimioterapia (n=130) en pacientes con CU avanzado o metastásico con determinadas alteraciones en FGFR que han progresado durante o después de uno o dos tratamientos previos, de los que al menos uno incluye un agente anti-PD-(L) 1. 1, [v]
En junio de 2023, en base a la recomendación del comité independiente de monitorización de la seguridad de los datos, el estudio THOR se interrumpió tras el análisis intermedio de eficacia y a todos los pacientes a quienes aleatoriamente se les había administrado quimioterapia (docetaxel o vinflunina) se les ofreció la oportunidad de recibir erdafitinib como tratamiento crossover. 1 Los resultados demuestran que se alcanzó una mediana de supervivencia global (SG) de más de un año en pacientes tratados con erdafitinib en el momento del corte de datos, lo que señala una mejora significativa en comparación con los pacientes del grupo de quimioterapia (12,1 frente a 7,8 meses; hazard ratio [HR], 0,64; intervalo de confianza [IC] del 95%, 0,44 a 0,93; P=0,0050). 1 El tratamiento con erdafitinib también mostró una mejora en la mediana de la supervivencia libre de progresión (SLP) en comparación con quimioterapia de 5,6 meses frente a 2,7 meses (HR 0,58; IC del 95%, 0,41 a 0,82; P=0,0002) y una tasa de respuesta global (TRG) confirmada del 35,3% frente al 8,5%. 1
Se observaron acontecimientos adversos (AA) graves relacionados con el tratamiento en el 13,3% de los pacientes que recibieron erdafitinib y en el 24,1% de los pacientes a los que se aleatorizó a recibir quimioterapia. 1 Se observaron AA de grado 3 o superior en el 45,9% de los pacientes que recibieron erdafitinib y en el 46,4% de los que recibieron quimioterapia. 1 Entre los pacientes tratados con erdafitinib, el 8,1% presentó AA relacionados con el tratamiento que condujeron a la discontinuación del mismo, frente al 13,4% de los pacientes que recibieron quimioterapia. 1 Se notificó el fallecimiento por acontecimientos adversos relacionados con el tratamiento de un paciente que recibía erdafitinib y de seis pacientes que recibían quimioterapia. 1 “La aprobación de erdafitinib por la CE refleja nuestro compromiso inquebrantable por transformar los resultados de las personas con carcinoma urotelial no resecable o metastásico”, ha afirmado el Dr. Kiran Patel, vicepresidente de Desarrollo Clínico en Tumores Sólidos de Johnson & Johnson Innovative Medicine. “De cara al futuro, esperamos poder proseguir con nuestros esfuerzos en investigación y desarrollo para ofrecer nuevas esperanzas y resultados más avanzados a un mayor número de pacientes”.