La EMA acepta la revisión de depemokimab para asma con inflamación de tipo 2 y rinosinusitis crónica con poliposis nasal.
- ComiteNetMD
- 31 de enero de 2025
- Alergología e Inmunología Clínica, Neumonología
- 0 Comments
28/01/2025
En caso de aprobarse, depemokimab se convertiría en el primer fármaco biológico de acción ultraprolongada con administración cada seis meses.
GSK ha anunciado que la Agencia Europea de Medicamentos (EMA, por sus siglas en inglés) ha aceptado para su revisión la solicitud de autorización de comercialización para el uso de depemokimab en dos indicaciones.
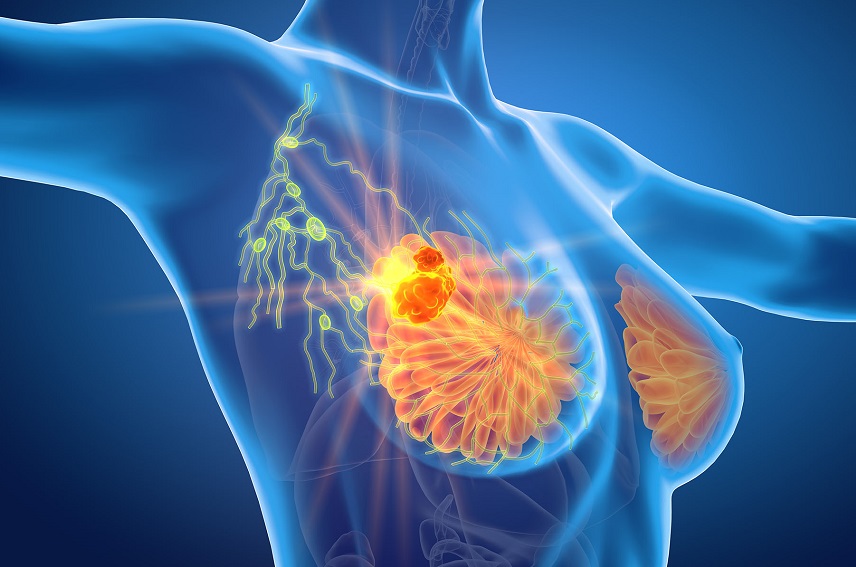
Las indicaciones solicitadas son para el tratamiento complementario de mantenimiento para el asma en pacientes adultos y adolescentes a partir de 12 años con inflamación de tipo 2 caracterizada por un fenotipo eosinofílico no controlado adecuadamente con dosis medias o altas de corticosteroides inhalados (CSI) más otro controlador del asma, y también como tratamiento complementario en pacientes adultos con rinosinusitis crónica con pólipos nasales (RSCcPN) no controlada.
Kaivan Khavandi, vicepresidente senior, y director global de Respiratorio/Inmunología I+D de GSK, ha declarado: “La presentación simultánea de la solicitud de autorización para ambas indicaciones pone de relieve nuestra confianza en depemokimab y su capacidad para ayudar a reducir la carga que suponen el asma y la RSCcPN para los pacientes y los sistemas sanitarios. Nuestros ensayos SWIFT y ANCHOR respaldan el potencial de este tratamiento para suprimir la IL-5, un conocido impulsor de la inflamación de tipo 2, con el fin de ofrecer a los pacientes la inhibición sostenida de un factor clave de su enfermedad, con sólo dos dosis al año.”
El fármaco, un anticuerpo monoclonal dirigido contra la interleucina-5 (IL-5), es el primer tratamiento biológico de acción ultraprolongada evaluado en ensayos de fase III con revisión regulatoria aceptada para su uso en estas afecciones.1 La vida media prolongada de depemokimab, su alta afinidad por la IL-5 y su potencia de unión a la IL-5, han respaldado los regímenes de dosificación de seis meses (26 semanas) basados en los resultados de los ensayos SWIFT y ANCHOR.1-3 En los pacientes asmáticos y en los que padecen RSCcPN, estos ensayos mostraron que depemokimab podía ofrecer la posibilidad de inhibir de forma sostenida un factor clave de su enfermedad y ayudar a conseguir resultados clínicos clave con un programa de dosificación de sólo dos inyecciones al año.1-3 Ha quedado demostrado que con intervalos más largos entre las dosis es posible superar los obstáculos para conseguir una atención óptima, entre ellos la adhesión del paciente.
La IL-5 es una citocina (proteína) clave en la inflamación de tipo 2.1,5,6 La inflamación de tipo 2 se identifica normalmente por el recuento de eosinófilos en sangre y es un factor subyacente en muchas enfermedades. Este tipo de inflamación está presente en la mayoría de los pacientes con asma grave y puede provocar exacerbaciones impredecibles y hospitalizaciones.,5,7 Este tipo de inflamación también está presente en hasta el 80% de las personas con RSCcPN y se asocia a una enfermedad y unos síntomas más graves.8-12
En Europa, se calcula que más de 42 millones de personas padecen asma, por lo que esta enfermedad supone una importante carga en la vida de esos pacientes y para los recursos sanitarios, con un coste social estimado en 46.000 millones de euros al año.13 La RSCcPN es una enfermedad crónica que afecta hasta al 4% de la población general, de la cual, un 40% no tiene controlada la enfermedad.8,9,12
Actualmente, depemokimab no está aprobado en ningún país.
Sobre el programa de desarrollo de depemokimab
El programa de fase III en asma con inflamación de tipo 2 consta de los ensayos SWIFT-1 y SWIFT-2, junto con un estudio de extensión abierto (AGILE).1,14 Se está llevando a cabo un estudio adicional (NIMBLE) para evaluar la eficacia y la seguridad de depemokimab en participantes con asma con inflamación de tipo 2 que cambian su tratamiento con mepolizumab o benralizumab.15
El programa de fase III en RSCcPN incluye dos estudios, ANCHOR-1 y ANCHOR-2.2,3
Depemokimab se está evaluando actualmente en ensayos de fase III para el tratamiento de otras enfermedades mediadas por la IL-5, como OCEAN para la granulomatosis eosinofílica con poliangitis (GEPA)16 y DESTINY para el síndrome hipereosinofílico (SHE).17
Sobre SWIFT-1 y SWIFT-2
SWIFT-1 y SWIFT-2 son ensayos clínicos de fase III multicéntricos, aleatorizados (2:1), doble ciego, controlados con placebo y de grupos paralelos, de 52 semanas de duración.1 Los ensayos han evaluado la eficacia y seguridad de la terapia complementaria con depemokimab en 382 y 380 participantes adultos y adolescentes con asma con inflamación de tipo 2 caracterizada por el recuento de eosinófilos en sangre, que fueron asignados aleatoriamente para recibir depemokimab o placebo, respectivamente, además de su tratamiento estándar con corticosteroides inhalados de dosis media a alta junto con, al menos, un controlador adicional.1 Número de sujetos incluidos en el conjunto completo de análisis de SWIFT-1: depemokimab = 250, placebo = 132 y en SWIFT-2: depemokimab = 252, placebo = 128.1
Estos resultados se han reportado y publicado en el New England Journal of Medicine.
Sobre ANCHOR-1 y ANCHOR-2
ANCHOR-1 y ANCHOR-2 son ensayos clínicos de fase III replicados que han evaluado la seguridad y eficacia de depemokimab en pacientes con RSCcPN. Ambos fueron ensayos multicéntricos, aleatorizados (1:1), doble ciego, de grupos paralelos, controlados con placebo y de 52 semanas de duración2,3. Número de sujetos incluidos en el conjunto completo de análisis de ANCHOR-1: depemokimab = 143, placebo = 128 y en ANCHOR-2: depemokimab = 129, placebo = 128.
Ambos estudios cumplieron sus criterios de valoración coprimarios de cambio respecto al valor basal en la puntuación total de pólipos nasales endoscópicos a las 52 semanas y de cambio respecto al valor basal en la puntuación media de la escala de respuesta verbal (ERV) de obstrucción nasal entre las semanas 49 y 52.
La incidencia global y la gravedad de los acontecimientos adversos emergentes del tratamiento en ANCHOR-1 y ANCHOR-2 también fueron similares en los pacientes tratados con depemokimab o con placebo.
Los resultados completos de ANCHOR-1 y ANCHOR-2 se presentarán en un próximo congreso científico.
Sobre el asma, la RSCcPN y la inflamación tipo 2
El asma afecta a más de 260 millones de personas en el mundo, muchas de las cuales continúan experimentando síntomas y exacerbaciones a pesar del tratamiento con altas dosis de corticosteroides inhalados más un segundo controlador (y/o corticosteroides sistémicos) o terapia biológica, para evitar que se “descontrole” o que permanezca “descontrolada” a pesar del tratamiento4,17. El asma representa una importante carga económica, ya que las exacerbaciones suponen una carga de recursos para los sistemas sanitarios debido a las visitas a urgencias y las hospitalizaciones18,20.
La RSCcPN está causada por una inflamación del revestimiento nasal que puede dar lugar a crecimientos de tejido blando, conocidos como pólipos nasales.9.12 Las personas con RSCcPN experimentan síntomas como obstrucción nasal, pérdida de olfato, dolor facial, trastornos del sueño, infecciones y secreción nasal que pueden afectar significativamente a su bienestar emocional y físico 9,12.
Hay pruebas que demuestran que la IL-5 tiene amplios efectos sobre otros tipos de células estructurales e inmunitarias, además de los eosinófilos, y cómo contribuyen a la inflamación, lo que puede provocar la remodelación pulmonar y la progresión de la enfermedad.5,6,21-25 Las investigaciones en curso están generando más pruebas para comprender las funciones de estas células y su posible contribución a los resultados clínicos en pacientes con enfermedades respiratorias. La inflamación de tipo 2 impulsa la disfunción subyacente de diversas afecciones inmunomediadas. La IL-5 es una citocina (proteína) esencial en la inflamación de tipo 2.5,6 La presencia de inflamación de tipo 2 en el asma o en la RSCcPN puede detectarse mediante el recuento de eosinófilos en sangre, que mide el nivel de un tipo de glóbulos blancos.5,8,12